对增强子、超级增强子相关研究作个汇总。
1 增强子鉴定
寻找目标增强子是研究增强子的第一步,也是引出下游分析及试验的开端。那么,如何寻找基因组中潜在的增强子区域呢?
组蛋白修饰的ChIP-seq分析
组蛋白修饰能预测染色质的类型、区分基因组功能元件,例如H3K4me1、H3K27ac通常在增强子区域存在富集。一般而言,当增强子区只有H3K4me1富集时,该增强子处于平衡状态;而当增强子区域同时富集H3K4me1和H3K27ac时,该增强子处于激活状态促进基因表达。
得益于高通量测序技术的发展,目前ChIP-seq试验已经广泛用于识别、鉴定增强子结构区。这种方法也是文献中的常规思路,灵敏度较高。
可再进一步通过富含谱系特异性TF、共激活因子以及组蛋白修饰标记H3K27ac等特征,区分增强子簇(称为超级增强子)与普通增强子。
数据库获取注释
例如ENCODE、FANTOM、HEP等,都能够获取增强子注释信息。它们是收集已知试验整理的,其中也广泛包含了ChIP-seq。
但数据库之间存在差异,并且增强子具有组织特异性,因此后续仍待鉴定。
2 增强子相互作用靶标的预测
仅识别增强子是意义不大的,重要的是找到增强子调控的下游基因,或者定位调控通路轴,通过基因或通路功能的改变以解释观察到的生物学现象或过程。
首先就是靶基因的预测。大多数情况下,通过已知增强子预测靶基因,方法有如下几种。并且在鉴定到候选的靶基因后,可再进一步结合组间(如处理组和对照组)差异基因表达列表,进一步定位关注的目标基因。
通过已知的数据库
例如SEdb,人类超级增强子相关的数据库,对于某特定超级增强子,存在几种类型的超级增强子-基因对应关系:
overlap gene:与超级增强子重叠的基因;
proximal gene:超级增强子邻近的基因;
closest gene:距离超级增强子最近的基因。
同时还包含了超级增强子来源的细胞、组织类型等信息,可据此获取超级增强子-基因关系对。
再如SEanalysis,可以根据超级增强子、细胞组织类型、转录因子、信号传导途径或基因进行搜索,获知超级增强子与相互作用基因或转录因子等的关系。
优点:信息丰富,准确、快速。
缺点:受数据库总量的限制。
根据基因注释,在增强子上下游位置寻找临近基因
如果增强子在基因组中的位置已知,可以根据已知的人基因组注释信息,在增强子上下游一定区域寻找相关的基因,如邻近基因、重叠的基因等,将它们视为直接的靶标。这种方法即基于“增强子与其邻近的mRNA启动子相互作用”这一观点。
优点:快速简单。
缺点:增强子存在远端调控,因此无法适用于距离很远但真实受到调控的靶基因。
基于增强子RNA和基因启动子的相关活性
某些增强子以RNA形式发挥作用,即eRNA,通常通过和转录因子结合调控靶基因。可通过检测eRNA与靶基因RNA之间的相关表达活性,若相关性很强,则可将基因视为该增强子的候选靶标。
如果有必要,也可以结合上述方法,指定一定的距离范围。
优点:可识别组织特异性的相互作用。
缺点:增强子eRNA和基因转录的RNA具有多对多的关系,如一个启动子可以与多个增强子关联,一个增强子也可以与多个启动子关联。并且无法有效识别eRNA和基因转录的RNA之间是直接还是间接的相互作用。
3 增强子活性测定及评估
在预测了增强子-基因对后,对于待继续研究的目标基因,验证相关的增强子是否对靶基因的表达产生影响。
常规的方法大致如下。
荧光素酶报告载体试验
可通过将候选增强子克隆至增强子报告载体中,若某增强子显著增加了荧光素酶的表达水平,则表明该增强子发挥功能。
基因干扰/敲除试验,基因获得试验
例如改造增强子结构区元件,敲低或过表达增强子RNA的表达水平等,检测相关靶基因的表达水平是否变化强烈,据此推断增强子是否发挥功能。
3C/5C/Hi-C等
这些技术通过捕获染色质构象,识别相互作用的DNA元件。若已知的增强子和某基因启动子区形成特定的DNA构象,如染色质环;或者信号强度明显大于相似距离的其它位置的DNA结构区,则可认为二者明显互作。
ChIP-seq
增强子通常募集转录因子来实现其增强子活性。因此可寻找一些与增强子相关的调控靶基因转录的转录因子,通过ChIP-seq,观察哪些已知的增强子和ChIP-seq峰重叠,以及鉴定有效的motif基序等。
4 相关研究解读
最后,让我们来结合几篇文献来看一下有关增强子的具体研究吧。
(1)增强子-编码基因的研究:
Lin L, Huang M, Shi X, et al. Super-enhancer-associated MEIS1 promotes transcriptional dysregulation in Ewing sarcoma in co-operation with EWS-FLI1. Nucleic Acids Research, 2019, 47(3): 1255-1267.
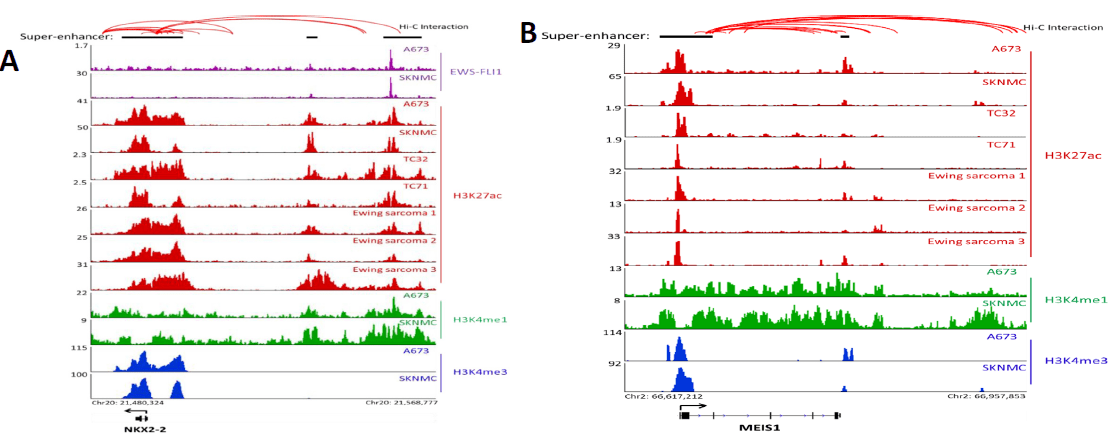
增强子-编码基因的研究
增强子相关的内容概要:研究人员发现THZ1抑制尤文肉瘤癌基因的表达。由于与超级增强子相关基因的表达需要持续的转录激活,它们特别容易受到转录抑制,因此猜测尤文肉瘤中的超级增强子可能为THZ1介导的选择性转录抑制提供机理解释。
超级增强子鉴定:研究人员分析了4个尤文肉瘤细胞系和3的原发性肿瘤的H3K27ac ChIP-seq数据,确定了超级增强子集。
超级增强子的靶基因鉴定:将距离增强子最近的基因视为增强子的直接靶标,并从中选择了在4个尤文肉瘤细胞系中出现频率大于3个细胞系以及在3个主要样本中至少出现1次的基因,共获得147个基因。其中许多是已知的尤文肉瘤癌基因,以及其它癌症类型的促生长因子。在这147个超级增强子相关基因的转录本中,研究人员重点关注了MEIS1,因为它在的超级增强子强度排在首位,并且它在尤文肉瘤中有突出的表达谱。
超级增强子功能验证:Hi-C分析表明增强子和候选靶基因启动子之间存在广泛的相互作用。萤光素酶报告基因检测显示MEIS1超级增强子活性强烈,免疫印迹证实了尤文肉瘤中MEIS1对THZ1处理具有高度敏感性。此外,荧光素酶报告基因试验还验证了主要发挥功能的的超级增强子元件。
(2)增强子-lncRNA的研究:
Lin X, Spindler T J, Fonseca M A, et al. Super-Enhancer-Associated LncRNA UCA1 Interacts Directly with AMOT to Activate YAP Target Genes in Epithelial Ovarian Cancer. iScience, 2019: 242-255.
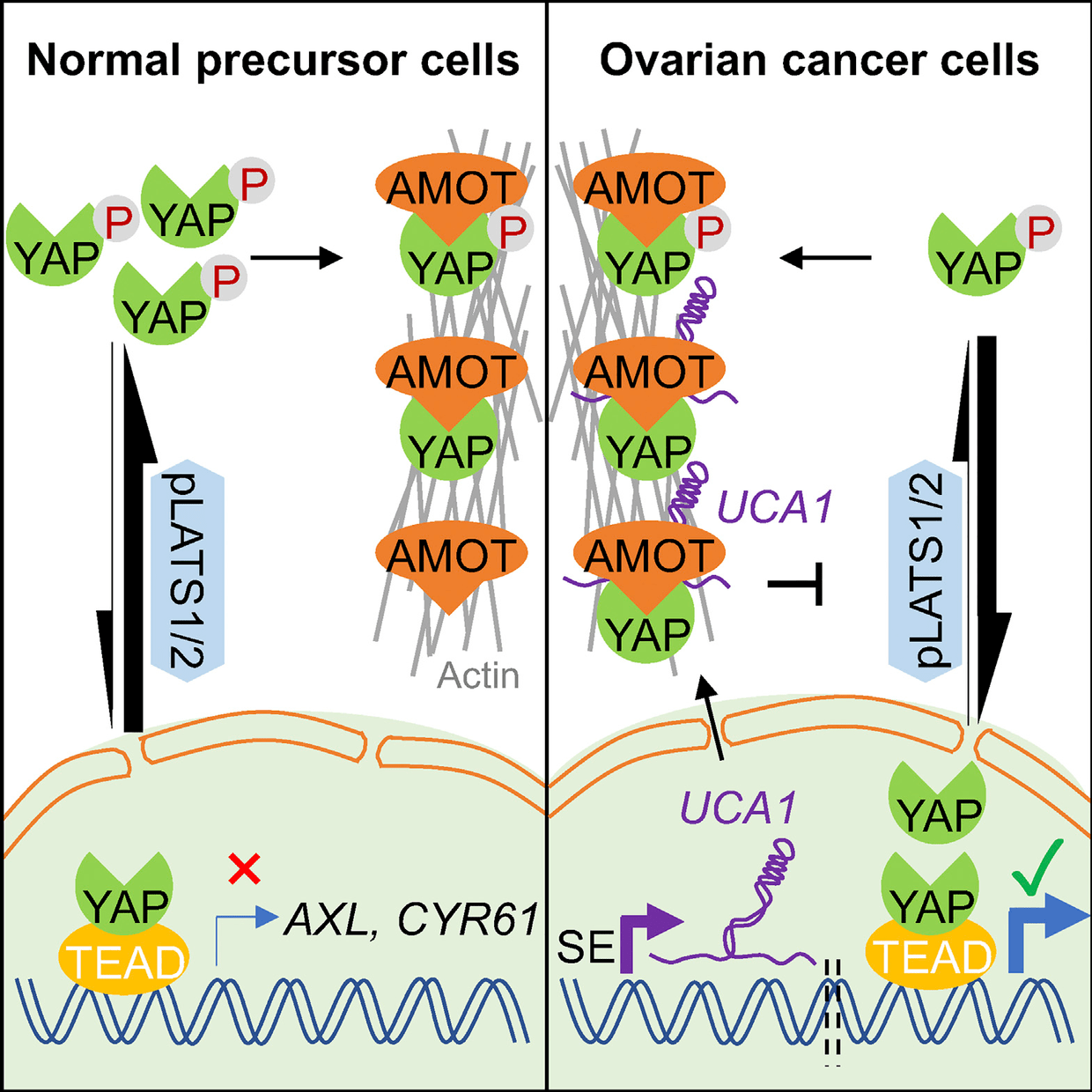
增强子-lncRNA的研究
增强子相关的内容概要:本篇研究鉴定了一种超级增强子相关的lncRNA UCA1,参与了卵巢癌的过程。
超级增强子鉴定:研究人员通过H3K27ac ChIP-seq数据鉴定超级增强子,并进一步选择了至少在两个高级浆液性卵巢癌样本中的超级增强子,以及在同一细胞系中与两个技术重复重叠的所有超级增强子以获得联合集。
超级增强子相关的lncRNA鉴定:在高级浆液性卵巢癌样本中将与超级增强子重叠的差异表达的lncRNA视为调控靶标,共得到93种与超级增强子表达相关的lncRNA。已知LncRNA UCA1参与多种癌症发生,UCA1与预后相关,并且UCA1在主要的卵巢癌组织类型中均表现出超增强子的特征以及与超级增强子信号呈正相关,推断肿瘤特异性超级增强子调节UCA1的表达。与超级增强子相关的基因对溴域蛋白BET家族的一种蛋白抑制剂(+)-JQ1的处理存在特殊的反应,UCA1同样表现出了这一特征。
(3)增强子-circRNA的研究:
Huang S, Li X, Zheng H, et al. Loss of Super-Enhancer-Regulated circRNA Nfix Induces Cardiac Regeneration After Myocardial Infarction in Adult Mice. Circulation, 2019, 139(25): 2857-2876.
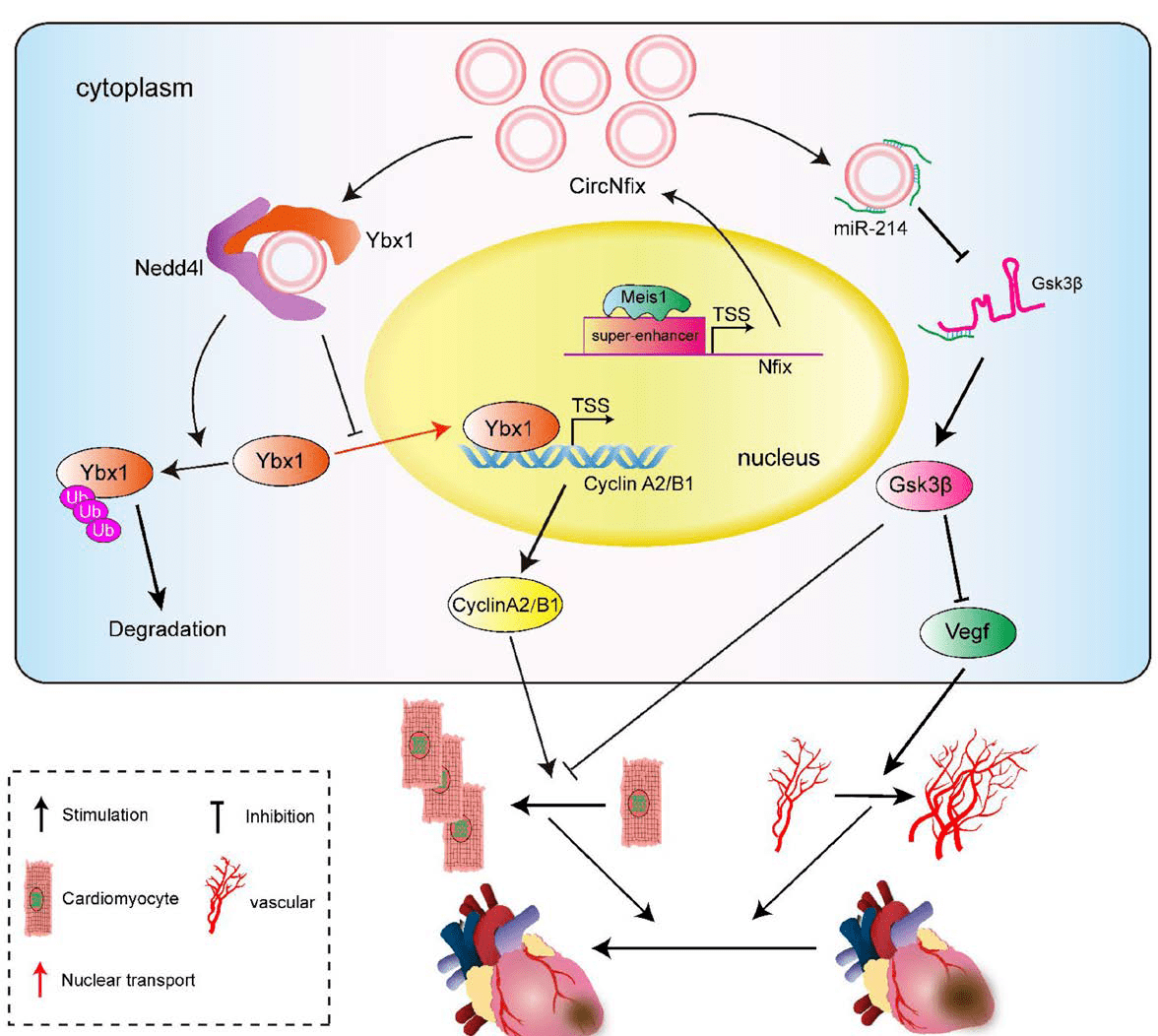
增强子-circRNA的研究
增强子相关的内容概要:本篇研究通过超级增强子确定了心脏再生调控中的关键circRNA,并探讨了circRNA功能的潜在机制。
超级增强子鉴定:研究人员通过H3K27ac标记,在23个人类组织样本中鉴定超级增强子。
超级增强子相关的circRNA鉴定:将增强子分配给最邻近的circRNA启动子,定义了超级增强子相关circRNA(SE-circRNA),进一步通过组织差异表达的circRNA,确立了心脏发育阶段特异性的SE-circRNA子集。观察到circRNA_Nfix(circNfix)在成年机体的心肌细胞中具有更高程度的富集,结合文献的相关报道,推测其可能参与了成年心肌细胞的增殖和心脏再生过程,并开始着手研究该超级增强子相关circNfix。
超级增强子功能验证:在验证了circNfix功能后,反过来定位具体哪个增强子与circNfix相关。通过ChIP-seq分析,确定了主要的超级增强子峰。染色质3C分析显示circNfix启动子和超级增强子之间存在染色质环,支持了超级增强子作为circNfix的调节元件。荧光素酶报告系统测定增强子活性,增强子E2被在心肌细胞中活性最强。
(4)增强子与SNP:
Shao L, Zuo X, Yang Y, et al. The inherited variations of a p53-responsive enhancer in 13q12.12 confer lung cancer risk by attenuating TNFRSF19 expression. Genome Biology, 2019, 20(1).
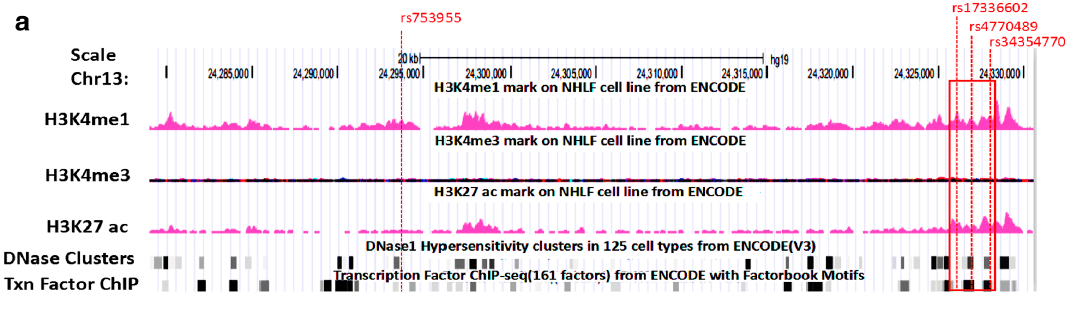
增强子与SNP
增强子相关的内容概要:本篇研究在rs753955的49-kb高连锁不平衡块中鉴定到肺组织细胞特异性新型p53响应增强子13q-Enh,其通过染色质环上调靶基因TNFRSF19保护细胞,13q-Enh的突变削弱了增强子的活性从而引发一系列致癌风险。
增强子鉴定:研究人员探索了GWAS SNP rs753955(A>G)附近促成肺癌风险的潜在增强子。首先确定了跨度49 kb的rs753955的LD区域,通过人肺成纤维细胞系数据,基于包括特定组蛋白标记,例如H3K4me1、H3K27ac的高富集和H3K4me3的低富集,DNase I超敏性环绕,以及转录因子的多个结合位点等确定假定的活性增强子。假定的增强子应在转录因子结合位点之内或附近包含常见的种系遗传变异,在rs753955的49 kb LD区段中鉴定出一个假定的增强子元件,13q-Enh。通过荧光素酶活性测定,13q-Enh在肺组织中显示出剧烈的增强子活性。使用抗H3K4me1和H3K27ac抗体的ChIP分析证实了13q-Enh上H3K4me1和H3K27ac的富集,这是活性增强子的组蛋白标记。H3K27ac ChIP-seq数据显示,13q-Enh在肺组织中富含H3K27ac,非肺组织13q-Enh中的H3K27ac含量则较低。据此判定13q-Enh是肺组织特异性的活性增强子。
增强子靶基因鉴定:肺组织样品的表达定量性状基因座(eQTL)分析显示,在风险SNP的2Mbp窗口内的所有基因中,只有TNFRSF19的表达与风险SNP rs753955显著相关,13q-Enh敲低的细胞中TNFRSF19表达降低超过50%。染色体3C分析证实了13q-Enh通过染色质环与TNFRSF19启动子发生特异性物理连接。据此推断TNFRSF19是增强子的潜在靶基因。
(5)增强子与SNP,增强子-启动子转换的双功能:
Hua J T, Ahmed M, Guo H, et al. Risk SNP-Mediated Promoter-Enhancer Switching Drives Prostate Cancer through lncRNA PCAT19. Cell, 2018, 174(3): 564-575.
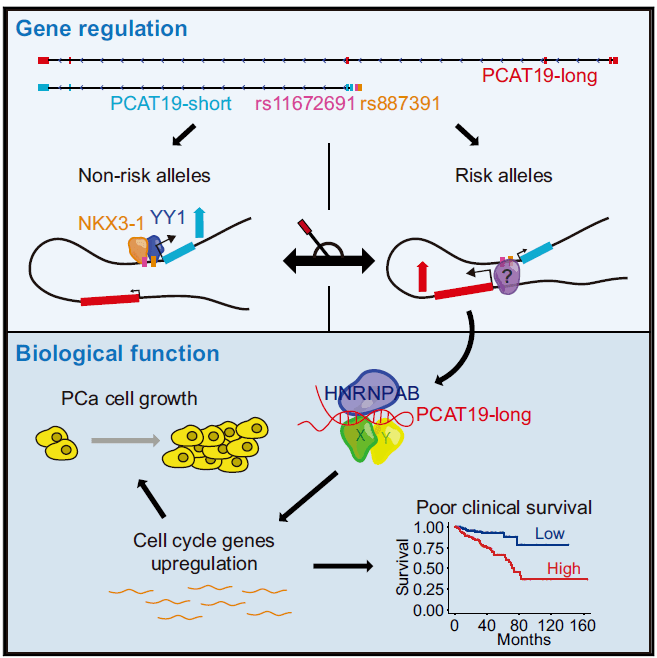
增强子与SNP,增强子-启动子转换的双功能
增强子相关的内容概要:前列腺癌(PCa)风险相关的SNP rs11672691,该SNP位点具有启动子-增强子双重活性,非风险SNP有更高的启动子活性,增强PCAT19亚型PCAT19-short的转录;风险SNP有更高的增强子活性,增强PCAT19亚型PCAT19-long的转录。
增强子鉴定:研究中通过H3K4me3和H3K4me1 ChIP-seq数据支持了该SNP区域具有与启动子和增强子均相关的组蛋白标记。
增强子功能验证:通过荧光素酶报告载体,支持了对双功能调节元件的假设。染色质3C分析鉴定到风险SNP区与PCAT19-long启动子存在更强的相互作用。
(6)增强子RNA的全基因组关联分析,增强子相关数据库:
Zhang Z, Lee J, Ruan H,et al. Transcriptional landscape and clinical utility of enhancer RNAs for eRNA-targeted therapy in cancer. Nat Commun, 2019, 10:4562
这种类型的大数据关联分析,整合了丰富的信息来源,通常是构建数据库的常规方法。我们可通过检索数据库资源,为研究提供有力的参考见解。
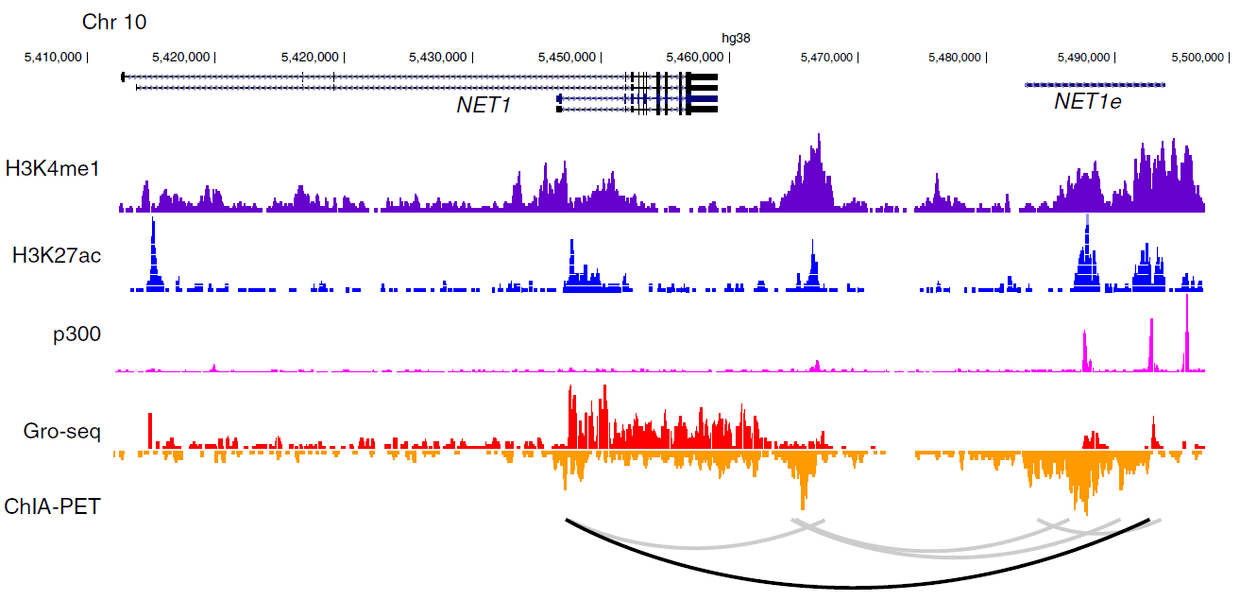
增强子RNA的全基因组关联分析
增强子相关的内容概要:该项研究大量收集公共数据,综合地在全基因组层面上分析了增强子RNA(eRNA)在各类癌症中的表达模式、eRNA与转录因子的结合、eRNA调控的靶基因预测、eRNA与临床特征的关系等,全方位地探索了eRNA在癌症中的系统结构和潜在功能。最后构建了癌症eRNA数据门户(eRic,<u>https://hanlab.uth.edu/eRic/</u>)
(7)通过转录因子定位增强子:
Kalna V, Yang Y, Peghaire C R, et al. The Transcription Factor ERG Regulates Super-Enhancers Associated With an Endothelial-Specific Gene Expression Program. Circulation Research, 2019, 124(9): 1337-1349.
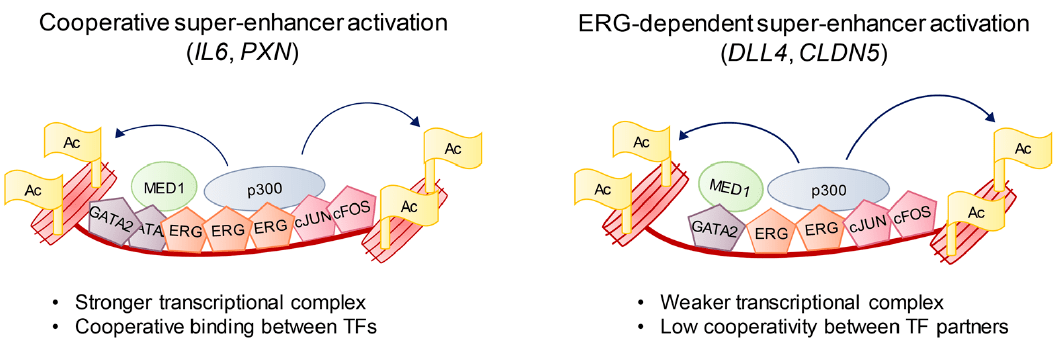
通过转录因子定位增强子
增强子相关的内容概要:该研究通过将转录因子ChIP-seq数据与标记增强子的组蛋白修饰数据进行关联,证明转录因子ERG通过调节超级增强子促进内皮稳态。
转录因子结合的增强子鉴定:通过ChIP-seq检查ERG结合的染色质位置,97%的ERG峰映射到DNase I超敏区域,对已知ERG靶基因的分析表明ERG在DNase I超敏区域处的位点与活性启动子(H3K4me3和H3K27ac)和增强子(H3K4me1和H3K27ac)的组蛋白标记位点重叠,ERG更倾向与HUVEC结合在活性增强子处。4种ERG结合的活性增强子,称为E1-E4 ,通过H3K27ac和H3K4me1在CDH5基因座两侧的TSS的23 kb区域内富集而被选择。通过荧光素酶试验,证实E4最活跃。
搜索微信公众号“纪伟讲测序- 本文固定链接: https://maimengkong.com/zu/1419.html
- 转载请注明: : 萌小白 2023年4月5日 于 卖萌控的博客 发表
- 百度已收录
