日前,Nature Communications 发表了来自军事医学科学院放射与辐射医学研究所研究员周钢桥课题组关于肝癌的最新研究。研究利用单细胞转录组测序绘制了原发性及转移性肝癌单细胞图谱,揭示了肝癌微环境的免疫细胞群体的构成并评估了慢性 HBV/HCV 感染与 T 细胞浸润和耗竭之间的关系。同时,研究还发现一群与肝癌进展及转移密切相关的 MMP9+ 肿瘤相关巨噬细胞(TAM),在其终端分化过程中转录因子 PPARγ 发挥重要的驱动作用。研究加深了对肝癌免疫微环境的理解,有助于开发新的免疫治疗策略。文中所使用的单细胞转录组测序服务由博奥晶典提供。

研究背景
肝细胞癌(Hepatocellular cancer, HCC)是最常见的原发性肝癌,也是导致癌症死亡的第三大原因。HCC 通常对化疗和放疗具有抗性,同时免疫检查点阻断剂等免疫疗法在肝癌方面的临床治疗选择也比较有限。因此,研究肝癌免疫微环境以及识别肿瘤发展与治疗相关的关键细胞群可以为肝癌治疗提供新的思路。
研究线路
 图1 技术路线
图1 技术路线
研究结论
1、原发及转移性 HCC 单细胞图谱
研究人员对来自 10 例原发性或转移性 HCC 患者的 4 种组织类型:原发肿瘤组织(PT)、癌旁(NTL)、门静脉癌栓组织(PVTT)及淋巴结转移灶组织(MLN)进行了单细胞转录组测序。共获得 71,915 个细胞,经过无偏的 SNN 聚类生成 53 个细胞亚型,分为肝细胞和胆管细胞、T/NK 细胞、髓系细胞、B 细胞、内皮细胞、成纤维细胞等主要细胞类型。研究者发现,相较于 NTL,PT 中的 T/NK 细胞占比显著降低,髓系细胞显著富集,PVTT 和 MLN 中的细胞组成与 PT 类似。
 图2 肝癌单细胞图谱
图2 肝癌单细胞图谱
2、抗肿瘤中央记忆T细胞在早期三级淋巴结构中富集
作者首先分析了 T/NK 细胞亚群,将其细分为 14 个亚群。大部分 CD8+T 细胞及 NK 细胞富集在癌旁组织,在原发肿瘤及转移灶中显著减少。此外,研究者发现在肿瘤组织中聚集一群中央记忆 T 细胞(TCM),利用多色免疫荧光染色发现这群细胞主要富集于早期三级淋巴结构(E-TLS)中,并进一步证实了 E-TLS 中 CD4+ TCM、CD8+ T 和 CD20+ B 的共聚集。作者结合 TCGA 数据库将 HCC 肿瘤分为 TLShigh 和 TLSlow, 发现 E-TLS 中 CD4+ TCM 和 CD20+ B 主要集中于 TLShigh 中,并且与良好的预后相关,表明其具有抗肿瘤活性。
作者利用不同病毒源性患者的数据进行分析发现大部分 T 细胞亚群主要浸润在由 HBV 感染引起的患者肿瘤中。进一步分析 HCC 中与 HBV 相关的瘤内细胞毒性 T 细胞(CTL)的耗竭状态,发现耗竭型 CTL 在 HBV 感染的患者中的比例要高于非 HBV/HCV 感染的患者,通过 TCGA 数据库及流式分析进一步证实了此发现。表明慢性 HBV/HCV 感染与 HCC 肿瘤中 CD8+CTL 的浸润及耗竭状态相关。
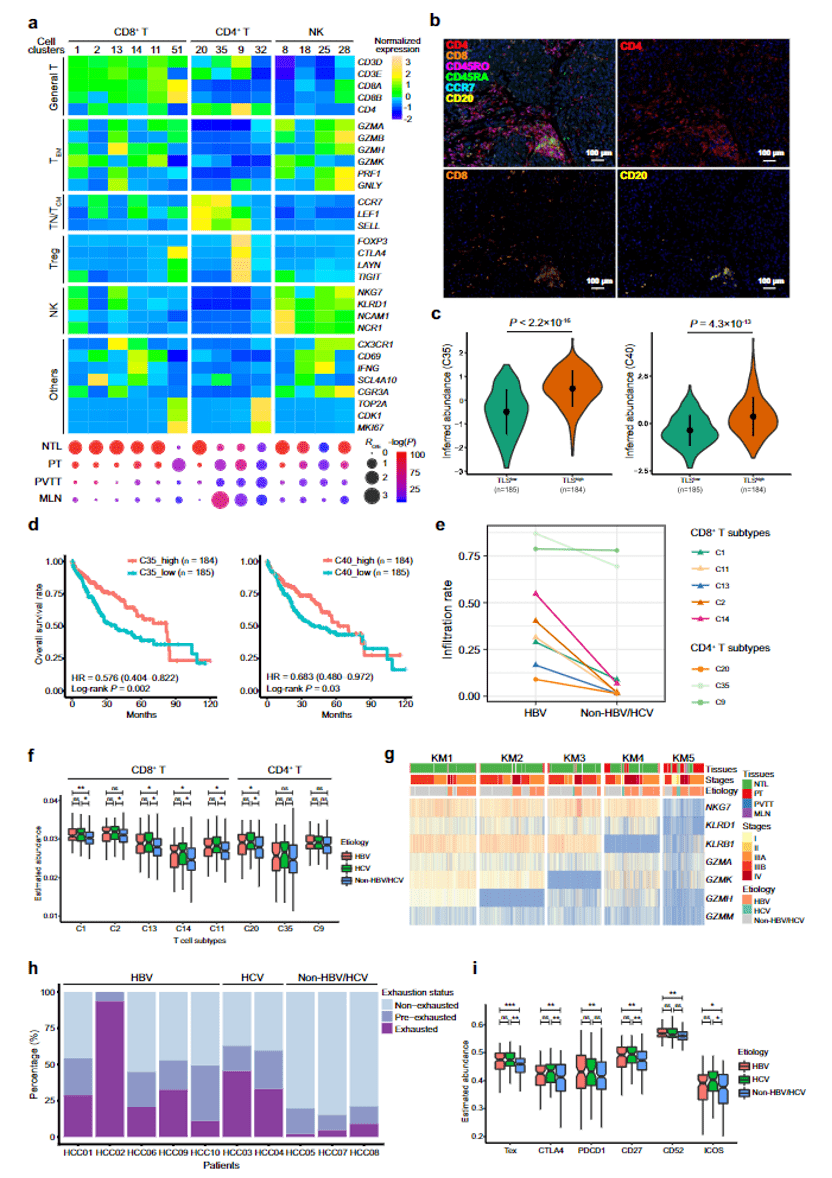 图3 HCC 中 T 细胞亚群分析
图3 HCC 中 T 细胞亚群分析
3、HCC 患者中瘤内巨噬细胞亚群分类
髓系细胞被细分为 14 个细胞簇,其中 11 群为巨噬细胞。不同样本中巨噬细胞的组成显示出较大的异质性,其中 MMP9+ 肿瘤相关巨噬细胞(TAM)与较差的的预后相关。作者利用流式分析及免疫荧光实验来进一步分析这群巨噬细胞在肿瘤进展中的作用,发现 PT 中 MMP9+ TAM 的占比要高于 NTL,同时 MMP9+ TAM 可以通过诱导 HCC 细胞的迁移、浸润和血管生成来促进 HCC 的进展。
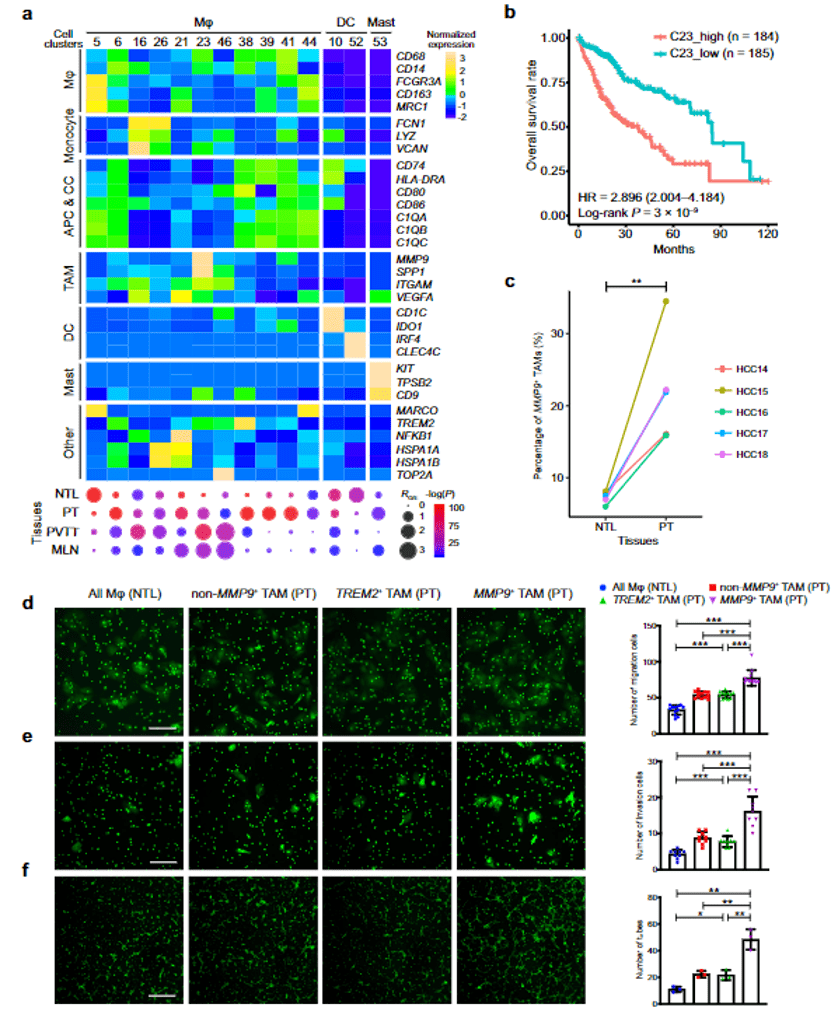 图4 肿瘤浸润的巨噬细胞的异质性分析
图4 肿瘤浸润的巨噬细胞的异质性分析
4、PPARγ 诱导 HCC 中巨噬细胞分化为 MMP9+TAMs
作者利用 StemID2 构建轨迹并结合 RNA 速率分析研究了巨噬细胞的分化,结果显示 MMP9+ TAMs 位于分化轨迹末端,并且分别由 MoMFs 巨噬细胞和 TREM2+ 巨噬细胞分化而来。通过 SCENIC 分析发现 PPARγ 是潜在的驱动巨噬细胞分化的关键的转录因子。后续的细胞培养实验证实 PPARγ 通过诱导 HCC 细胞迁移、侵袭和肿瘤血管生成来促进 HCC 发展,对 MMP9+ TAMs 的终端分化起关键作用。
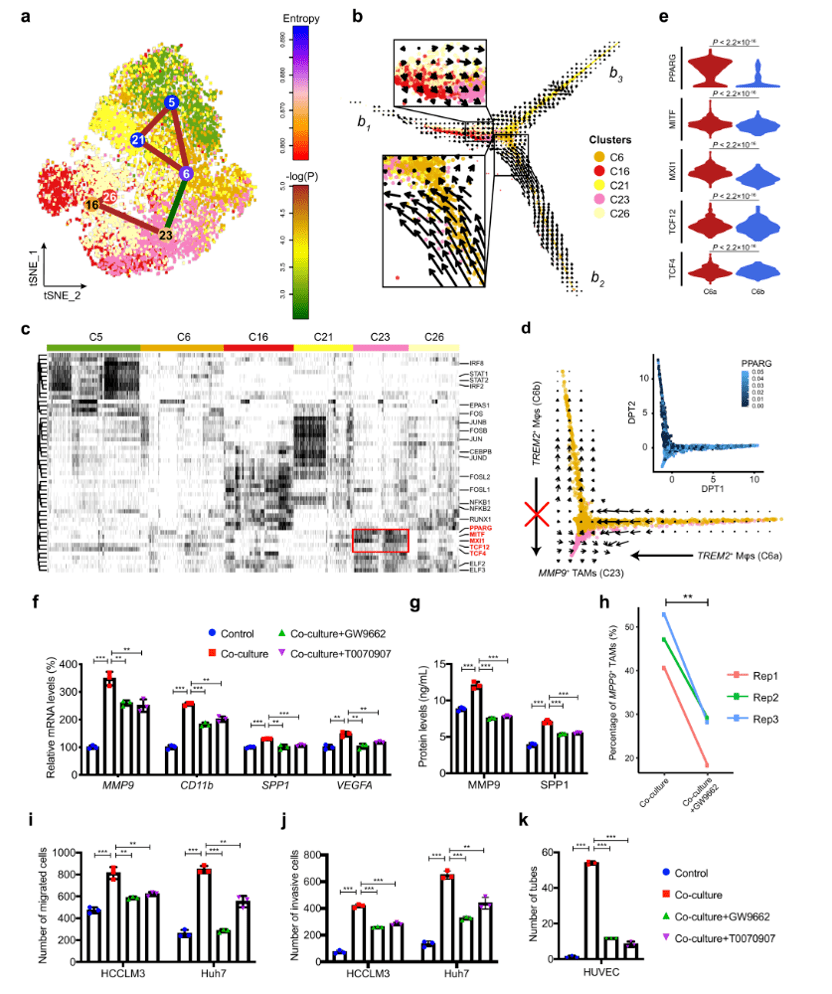 图5 PPARγ 诱导巨噬细胞分化为 MMP9+ TAM
图5 PPARγ 诱导巨噬细胞分化为 MMP9+ TAM
5、恶性肝细胞的瘤内转录组和基因组异质性
肝细胞被分为 14 个细胞簇,其中 12 个为恶性细胞亚群,分为促肿瘤生成肝细胞群和促肿瘤转移肝细胞群。其中,促肿瘤转移肝细胞具有较强的肿瘤细胞干性。作者利用促肿瘤转移肝细胞中的特征基因来对 HCC 肿瘤进行评级,发现促肿瘤转移评分越高,患者的生存预后越差。InferCNV 分析显示不同 HCC 患者具有不同的亚克隆突变,表明恶性肝细胞具有广泛的瘤内异质性。
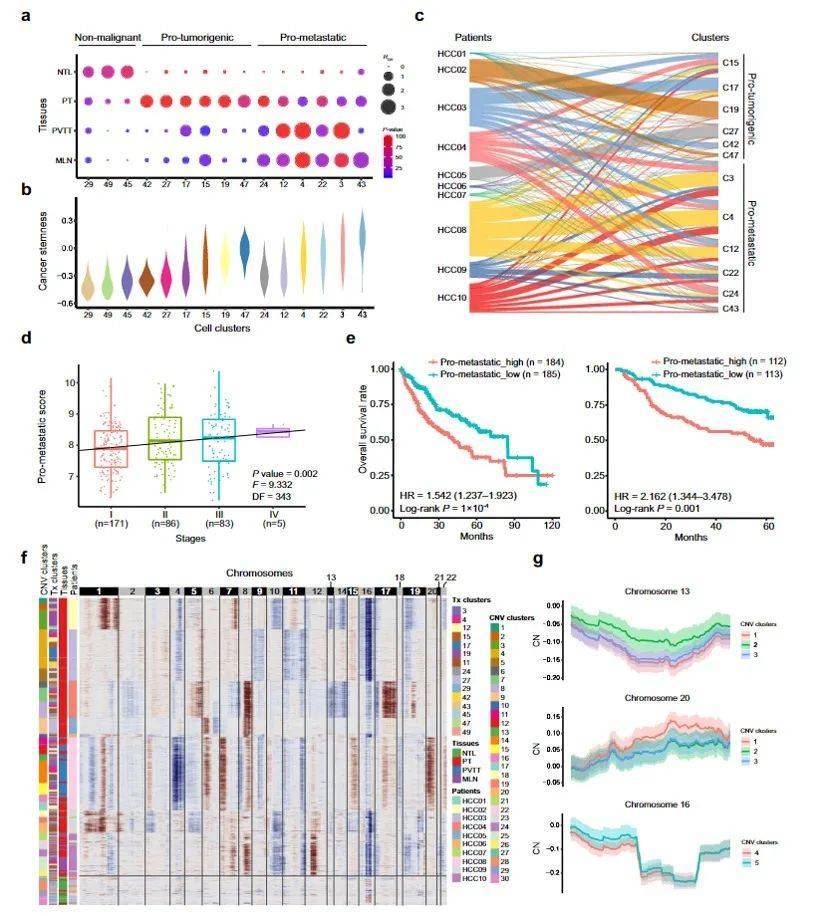 图6 恶性肝细胞的瘤内异质性
图6 恶性肝细胞的瘤内异质性
6、恶性肝细胞可以重塑 HCC 的微环境
作者利用 cellphoneDB 进行了细胞互作分析,发现 PT 中肝癌细胞内配体的大量产生会引起肝细胞相关的受配体对显著富集,而配体的表达水平可以很好地区分非恶性、促肿瘤生成及促肿瘤转移肝细胞,且不同类型肝细胞中激活的配体发挥不同的功能。在非恶性肝细胞中激活的配体参与肝细胞生理功能相关通路如生物代谢、脂肪酸和胆汁酸、脂肪生成等;促肿瘤生成肝细胞中的配体参与压力反应相关通路如炎症反应、干扰素、p53 及凋亡等;促肿瘤转移肝细胞中的配体参与 EMT、MYC、Notch 和肌细胞生成相关通路。作者进一步分析了促肿瘤生成和促肿瘤转移肝细胞中的受配体对,结果显示促肿瘤生成肝细胞与 T 细胞间的显著互作对(CXCL10/CXCR3、CXCL10/DPP4、CXCL11/CXCR3 和 CXCL11/DPP4)主要与炎症相关;而促肿瘤转移肝细胞与免疫细胞间的互作对(CCL20/CCR6、PTDSS1/JMJD、RPS19/C5AR1 和 MIF/CD74)主要与免疫抑制相关,表明促转移肝细胞在 HCC 免疫抑制微环境中发挥重要的作用。
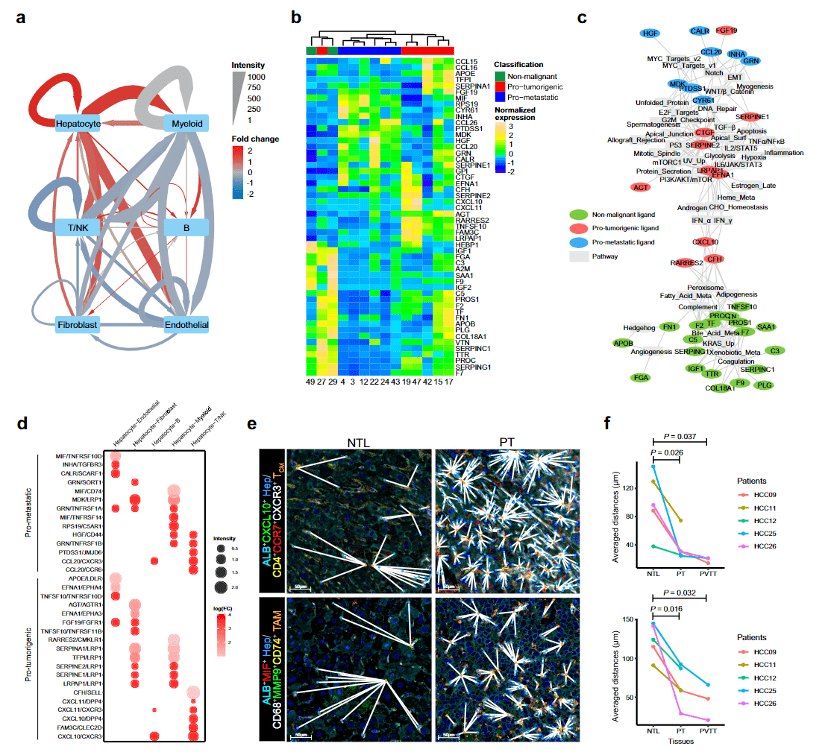 图7 恶性肝细胞对 HCC 肿瘤微环境的形成起重要作用
图7 恶性肝细胞对 HCC 肿瘤微环境的形成起重要作用
7、Bulk 数据的解卷积分析显示 HCC 中存在7个肿瘤微环境(TME)亚型
作者利用 TCGA 数据库中 HCC 的 bulk RNA-seq 数据分析识别了 HCC 中 7 个 TME 亚型。其中以巨噬细胞主导的 TME2 和 TME5 显示出较差的预后,同时这 2 个 TME 分别由较高比例的 MMP9+ TAM 以及 VEGFA+ TAM 组成。而主要由 CTLs、Tcm 和 CD20+B 细胞组成的 TME7 亚型预后较好。相对于 TME7 有更高占比的 CTLs 和抑制性 Treg 细胞的 TME3 则预后效果稍差,主要是由于 TME3 中有较多的干扰素生成 NK 及T细胞。
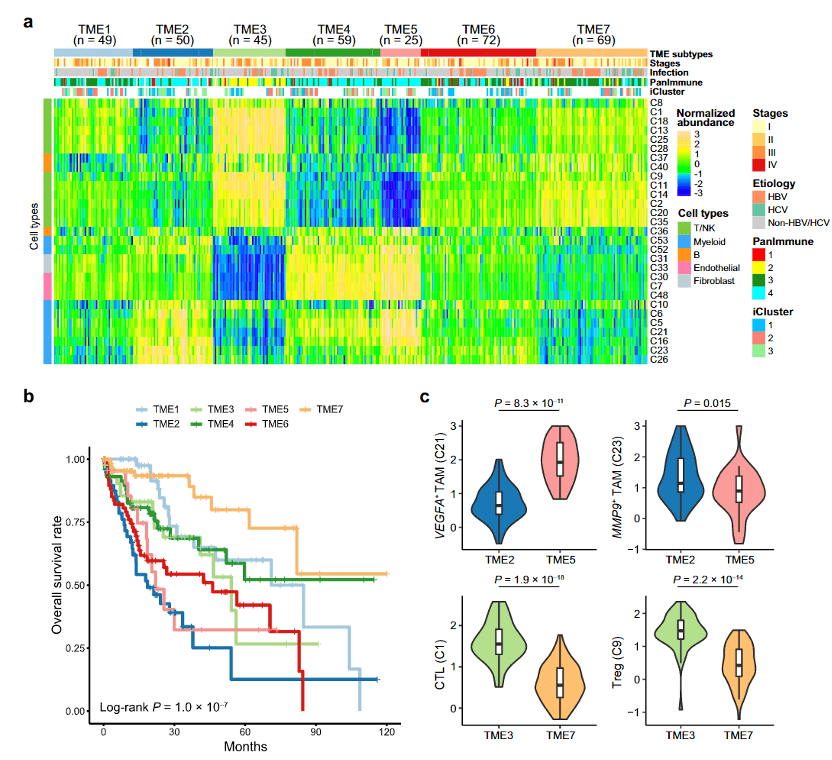 图8 结合 TCGA 分析获得 HCC 的 7 个 TME 亚型
图8 结合 TCGA 分析获得 HCC 的 7 个 TME 亚型
研究结论
本项研究对 HCC 患者不同组织部位 TME 的全面分析显示出在 HCC 微环境中的免疫和恶性细胞的异质性,揭示了 HCC 微环境中髓系和淋系细胞的差异谱系和迁移关系。这些研究结果可以进一步加深我们对于肝癌肿瘤微环境的理解,为未来肝癌的精准免疫治疗提供了重要的参考。
参考文献:
Lu Y, Yang A, Quan C, et al. A single-cell atlas of the multicellular ecosystem of primary and metastatic hepatocellular carcinoma. Nat Commun. 2022; 13(1): 4594. doi: 10.1038/s41467-022-32283-3.
转自:博奥晶典
- 本文固定链接: https://maimengkong.com/zixun/1501.html
- 转载请注明: : 萌小白 2023年4月30日 于 卖萌控的博客 发表
- 百度已收录
