撰写:生信小师妹 来源:小张聊科研平台的“ i生信”公众号,微信公众号搜索“ i生信”即可关注/扫描关注见文末
#生信分析# #生信发文# #miRNA#
自从1993年发现第一个miRNA以来,miRNA相关文章已经发表了15W+,且研究思路主要是基于miRNA的经典机制(详见正文——大多数人看到的miRNA),以至于持续研究20多年后,miRNA已然成了过气明星。
同样的,20多年的研究基础,手里握着miRNA数据的科研人也构成了miRNA庞大的粉丝基础,过气明星要翻红即有需求又有可行性,尤其是当初步分析/实验的结果无法用经典机制进行解释时,就需要考虑是否可以用非经典机制进行解释,这样做即可以提高数据的可用性又可以增加研究的创新性。今天介绍一种研究还比较少创新性比较高的miRNA非经典机制——NamiRNA。

大多数人看到的miRNA
MicroRNAs(miRNAs)是一种长度约为22个核苷酸的RNA,在真核生物中参与靶mRNA的转录后抑制。这一过程发生在细胞质中,miRNA对基因的表达起着负调控的功能,即为miRNA的经典机制模式。
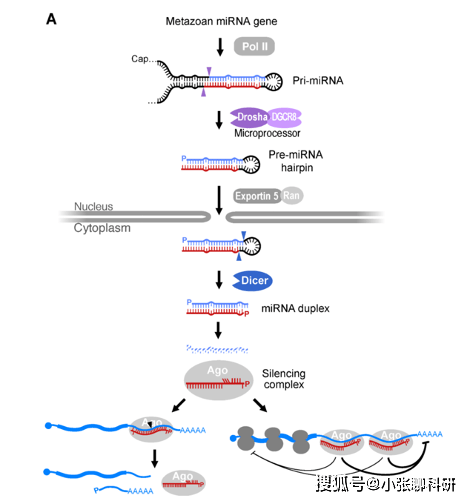 经典miRNA的生物发生和功能(DOI: 10.1016/j.cell.2018.03.006)
经典miRNA的生物发生和功能(DOI: 10.1016/j.cell.2018.03.006)
在真核生物中,Pol II酶转录生成的pri-miRNA自身折叠形成发夹结构,该结构进一步裂解形成pre-miRNA ,进而被运输到到细胞质中。
在细胞质中,pre-miRNA被Dicer内切酶切割产生一个约20 bp的miRNA双链,随后其中一条链降解,零一条链作为成熟的miRNA与Ago蛋白结合形成沉默复合体。
在沉默复合体中,miRNA与靶mRNA的3’-UTR结合,进而使得靶mRNA被降解、稳定性降低、翻译效率降低,造成转录后抑制,最终降低靶蛋白的表达水平。
少数人看到的miRNA
除了上述经典的、大家研究比较多的、研究思路较为成熟的miRNA调控外,Cell的Snapshot系列也总结了多种miRNA非经典调控机制。
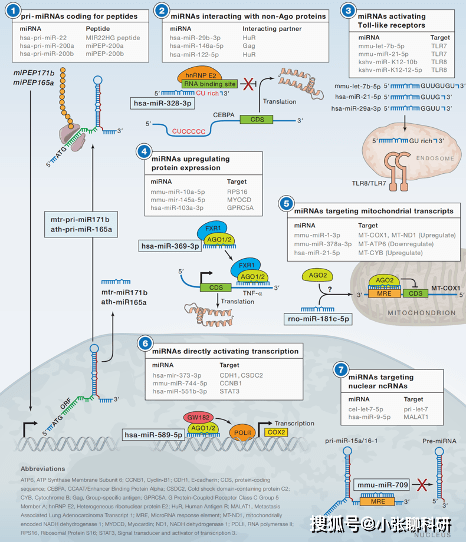 miRNA的非经典机制(DOI: 10.1016/j.cell.2018.07.040)
miRNA的非经典机制(DOI: 10.1016/j.cell.2018.07.040)
① pri-miRNA 可编码多肽
部分pri-miRNA可以编码调控肽,这些调控肽被称为miRNA编码肽(mipep),其功能是通过增加其自身pri-miRNA的转录,进而增强了其相应成熟miRNA的积累。
② miRNA 与非AGO 蛋白相互作用
在miRNA的经典机制中,mRNA是要与Ago蛋白结合形成沉默复合体的,但是研究发现,除了AGO蛋白外,miRNA也可以和其他蛋白结合进而发挥作用。
③激活 Toll 样受体
miRNA可以作为激动剂激活 Toll样受体,这种激动剂在肺癌中引起转移性炎症反应,阻断这种激动剂作用可能对患者具有治疗意义。
④ miRNA 可上调蛋白的表达
部分miRNA对蛋白表达的影响方向可能是细胞周期依赖的,即特定的miRNA在细胞周期阻滞时诱导目标mRNA的翻译,但在增殖细胞中起到抑制翻译的作用。
⑤miRNA 可靶向线粒体转录本
miRNA的经典机制是发生在细胞质中的,尽管尚未在线粒体基因组中发现miRNA,但是有研究表明miRNA可转位到线粒体中,抑制或增加线粒体基因的翻译。这类miRNA也是靶向治疗以恢复正常的线粒体功能的潜在靶点。
⑥miRNA直接激活转录
非经典的miRNA也可进入细胞核中发挥作用,通过与靶基因的启动子结合,进而诱导靶基因的表达。
⑦ miRNA 靶向核内的ncRNAs
部分具有细胞核定位功能miRNA可以抑制其他miRNA的成熟。
于文强老师看到的miRNA
在上述7种miRNA的非经典机制之外,复旦大学于文强实验室于2017年提出了一种新的miRNA调控机制——NamiRNA(Nuclear activating miRNA) 通过与靶基因的增强子结合,进而激活靶基因的表达。这一过程发生在细胞核中,miRNA对基因的表达起着正调控的功能,且需要增强子作为媒介。
 首次提出NamiRNA调控机制(DOI: 10.1080/15476286.2015.1112487)
首次提出NamiRNA调控机制(DOI: 10.1080/15476286.2015.1112487)
本研究中,作者发现miR-24-1通过靶向增强子激活了基因的转录。当增强子序列被TALEN敲除时,激活作用被完全取消。此外,作者发现miR-24-1激活增强子RNA (eRNA)表达,改变组蛋白修饰,并增加增强子位点上p300和RNA Pol II的富集。由此,作者提出了miRNA作为增强子触发的一种新的机制,即NamiRNA调控机制。
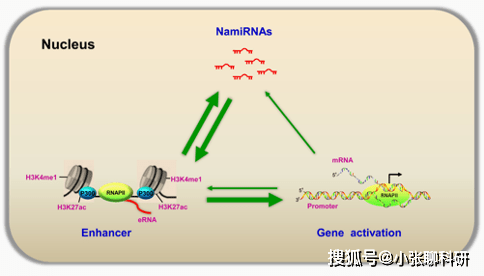 NamiRNA-增强子-靶基因激活网络模型(DOI: 10.1016/j.gpb.2017.05.001)
NamiRNA-增强子-靶基因激活网络模型(DOI: 10.1016/j.gpb.2017.05.001)
NamiRNA可以与增强子相互作用并激活,增强子也能激活内源性NamiRNA和近端基因的表达。因此,增强子和NamiRNA形成了一个正反馈网络。组织特异性转录因子有时可能通过靶向NamiRNA的启动子来调节其表达,或参与增强子激活的过程。作者提出了这样一个NamiRNA -增强子-靶基因激活网络模型,以便可以更好地理解NamiRNA 和增强子在调控基因转录过程中的crosstalk。
随着对NamiRNA研究的深入,作者进一步发现NamiRNA在细胞发育过程中激活基因表达,从而能够控制细胞命运。
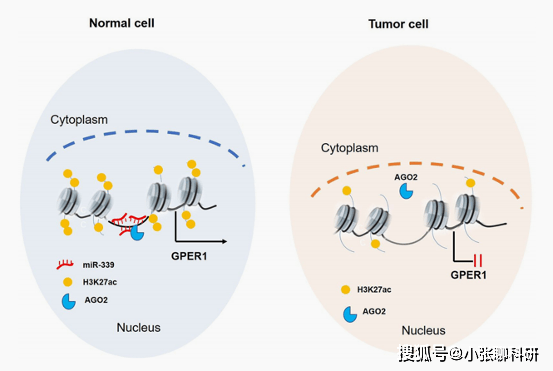 乳腺癌中NamiRNA调控模型(DOI: 10.1093/nar/gkab626)
乳腺癌中NamiRNA调控模型(DOI: 10.1093/nar/gkab626)
本研究中,作者发现在正常乳腺细胞中,NamiRNA miR-339与AGO2共定位并结合在增强子区域,激活抑癌基因GPER1表达,保护正常细胞不向恶性细胞转化。然而,当下调miR-339的表达,降低增强子活性时,相应的抑癌基因GPER1将被沉默,无法发挥其对肿瘤发生的抑制作用。
NamiRNA研究概况
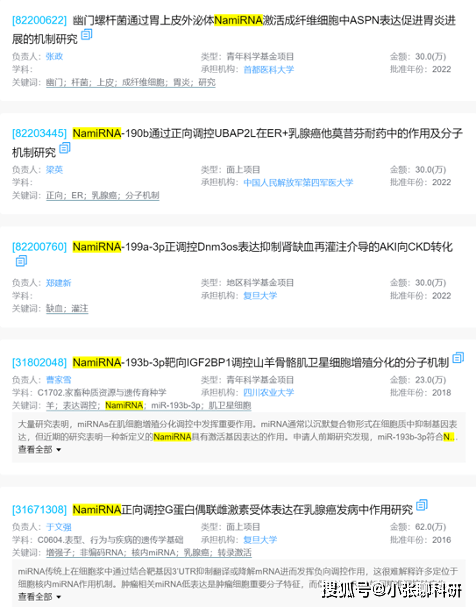
尚未被大众所熟知的NamiRNA,目前已发表文章还比较少,但是也成功助力了多项中标基金项目,其中2022年NamiRNA相关中标基金就有3个。
写在最后
如何将NamiRNA放到基金申请中,进而提高创新性:
·使用NamiRNA机制,筛选主角NamiRNA及下游靶基因;
·筛选诊断/预后等相关NamiRNA;
·筛选主角基因的上游NamiRNA。
如何将NamiRNA放到生信文章中,进而提高创新性:
·主角基因的上游调控机制预测方向中关注NamiRNA方向;
·NamiRNA作为科研热点,转化成可直接成文的分析思路(分析思路有哪些?详见近期i生信公众号所推荐的生信发文思路,或扫码咨询工作人员)。
原文链接:https://mp.weixin.qq.com/s/VFcs7qC9XsiUmSPE5qLlQQ- 本文固定链接: https://maimengkong.com/kyjc/1444.html
- 转载请注明: : 萌小白 2023年4月15日 于 卖萌控的博客 发表
- 百度已收录
